گیاه دارویی سیر – قسمت سوم
تیر ۱۲, ۱۳۹۸
گیاه دارویی سیر – قسمت چهارم
تیر ۱۲, ۱۳۹۸تداخل دارو با سایر داروها (Drug-Drug interaction)
امروزه استفاده از دارو به خصوص در کشورهای پیشرفته رشد چشمگیری داشته است. تخمین زده شده است که تقریباً ۸۰ درصد افراد بالغ در ایالات متحده آمریکا، حداقل یک دارو (داروهای تجویزی، داروهای بدون نسخه (OTC)، داروهای گیاهی) در هفته مصرف می کنند و این میزان، با بالا رفتن سن افزایش می یابد (۱). یک نظرسنجی اخیر در ایالات متحده، نشان می دهد که میانگین مصرف داروهای تجویز شده در هر بیمار، ۲/۳ عدد دارو می باشد (۲). استفاده همزمان، از بیش از یک دارو، می تواند منجر به بروز تداخلات دارویی گردد. تداخلات دارویی زمانی رخ می دهد که پاسخ بیمار به دارو در حضور یک داروی دیگر، مواد غذایی / نوشیدنی ها، ترکیبات گیاهی یا برخی عوامل محیطی تغییر یابد (۳).
اهمیت این نوع تداخلات دارویی با اولویت بالینی در ابتدا شامل شناخت یا پیش بینی بروز یک تداخل دارویی و عواقب ناشی از آن برای بیمار است. تداخلات دارویی ممکن است منجر به: ۱- کاهش یا افزایش اثر دارو(ها) شوند، ۲- افزایش واکنش های جانبی دارو (Adverse drug reactions) گردند و یا ۳- حتی ممکن است به دنبال بروز تداخل دارویی نیاز به ترک مصرف یکی از داروها باشد (۳, ۴).
جدول ۱. عوامل خطرزای شناخته شده در بروز تداخلات دارویی (۳, ۵)

عوامل خطرزا در بروز تداخلات دارویی را می توان به ۴ دسته تقسیم کرد: ۱) تجویز همزمان با داروهایی که دارای شاخص درمانی باریک (Narrow therapeutic index) و محدود هستند یعنی حاشیه کوچکی بین سطوح درمانی و سمیت دارو وجود دارد. ۲) داروهایی که دارای منحنی دوز- پاسخ شیب داری (Steep dose- response curve) هستند، یعنی افزایش کوچکی در سطح دارو منجر به افزایش شدید در اثر دارو می شود. ۳) داروهایی با داروهای که دارای متابولیسم کبدی اشباع پذیر (Saturable hepatic metabolism) هستند در صورت وجود تداخلات دارویی، احتمال تجمع آنها بسیار بالا می باشد. ۴) داروهایی که به صورت وابسته به دوز روی پاسخ بیمار (Dosage dependent on patient response) تأثیر می گذارند. (جدول ۱). بنابراین برای کاهش عوارض ناشی از تداخلات مصرف این نوع از داروها، نیاز به توجه دقیق هم از جانب پزشک در هنگام تجویز دارو و هم هنگام مصرف آن توسط بیمار دارد.
برخی از خصوصیات بیمار می تواند در بروز تداخلات دارویی (دارو- دارو) نقش داشته باشد. به عنوان مثال افزایش سن و زمینه های ژنتیکی عوامل مهم در بروز تداخلات دارویی محسوب می شوند. همچنین افزایش مصرف چند دارو به صورت همزمان، خطر بروز تداخلات دارویی را افزایش می دهد. به عنوان مثال احتمال بروز تداخلات دارویی در بیمارانی که بین ۲ تا ۵ دارو همزمان مصرف می کنند، ۱۹ درصد تخمین زده شده است؛ درحالی که این احتمال برای کسانی که ۶ دارو همزمان مصرف می کنند بیش از ۸۰ درصد تخمین زده می شود (۶). در حال حاضر مشخص شده است که مصرف همزمان بیش از ۵ دارو (Polypharmacy) اغلب نیازمند مدیریت ویژه ای در مصرف آنها توسط بیمار دارد (۴). با این وجود، افراد مبتلاء به بیماری های مزمن و یا ارثی ممکن است بیشتر در معرض عوارض جانبی ناشی از تداخلات بالقوه دارویی باشند، زیرا بیماری زمینه ای باعث اختلال در سازوکارهای هوموستازی آنها می شود (۷).
مکانیسم بروز تداخلات دارویی (دارو – دارو):
تداخلات دارویی (دارو – دارو) معمولاً توسط فرآیندهای فارماکودینامیک یا فارماکوکینتیک ایجاد می شوند.
تداخلات فارماکودینامیکی: این تداخلات معمولاً شامل اثرات هم افزایی (Additive)، هم نیرو زادی (Synergistic) یا آنتاگونیستی داروهایی هستند که بر روی گیرنده های مشابه یا سیستم های فیزیولوژیک اثر می گذارند. همچنین قسمت دیگری از تداخلات فارماکودینامیکی مربوط به تغییرات در تعادل الکترولیت ها و حجم مایع خارج سلولی می باشد. (۳). تداخلات فارماکودینامیکی رایج هستند اما همیشه شناخته شده نیستند. جدول ۲ برخی از این نوع تداخلات را نشان می دهد. تداخلات فارماکودینامیک، معمولاً زمانی قابل پیش بینی و مدیریت است که فارماکولوژی داروهای همزمان تجویز شده شناخته شود (۶).
جدول ۲. برخی از تداخلات رایج فارماکودینامیکی (۳, ۶)

تداخلات فارماکوکینتیکی: این تداخلات هنگامی رخ می دهند که یک دارو بر جذب، توزیع، متابولیسم (حذف) و دفع داروی دیگر تأثیر بگذارد. این امر موجب تغییر غلظت پلاسمایی (افزایش یا کاهش) یا تغییر در مدت زمان اثربخشی (افزایش کلیرنس یا انباشت) دارو شده و متعاقباً می تواند سبب کاهش کارآیی یا افزایش سمیت دارو شود (۶). تداخلات فارماکوکینتیکی در فعالیت های بالینی مؤثر است (جدول ۳).
جدول ۳. نمای کلی از اثرات بلقوه بالینی مرتبط با تداخلات فارماکوکینتیکی (۸, ۹)
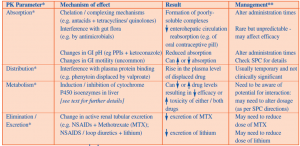
* القاء / مهار P-glycoprotein از داروی تحت تأثیر قرار گرفته در سلول در چند مرحله فارماکوکینتیکی تحت شرایط in vivo
** خلاصه ای از مشخصات محصول (SPC) برای هر دارو و اطلاعاتی در مورد پتانسیل تداخلات دارویی ارائه می دهد.
مشکلات مربوط به جذب معمولاً شامل بیش از یکی از مکانیسم های مشخص شده که در جدول ۳ ارائه شده می شود. در گذشته تصور می شد که مداخله با اتصالات پروتئین های پلاسما عواقب جدی در پی دارد، اما اکنون مشخص شده است که اکثر داروها به طور گسترده متصل به پروتئین های پلاسما هستند و به این صورت جا به جا می شوند (به عنوان مثال وارفارین، فنیتوئین، متوترکسات) همچنین دارای یک سیستم پاکسازی (کلیرنس) جبرانی هستند. بنابراین هر گونه افزایش در داروهای آزاد، موقتی است (۳, ۵). شایع ترین نوع تداخل در اثر حذف، شامل تغییر در دفع کلیوی یکی از داروها توسط داروی دیگر می باشد (جدول ۳). تداخلات دارویی معمولاً تمایل به دخالت در مکانیسم دفع صفراوی ندارند. بیشترین اهمیت تداخلات دارویی به لحاظ بالینی شامل تغییر در سرعت متابولیسم دارو یا داروهای تحت تأثیر قرار گرفته است (۳).
خانواده آنزیم های سیتوکروم پی ۴۵۰ (CYP450) نقش مهمی در متابولیسم دارند. این خانواده شامل تعداد زیادی از آنزیم های اکسیداتیو درگیر در بیوسنتز و تخریب بسیاری از مواد درونزاد (مثل چربی ها، ویتامین ها، استروئیدها) می باشند (۱۰). کبد محل اصلی فعالیت آنزیم های سیتوکروم است، اما این آنزیم ها در روده (جایی که می توانند بر فراهمی زیستی دارو اثر بگذارند)، کلیه ها، پوست، ریه و جفت نیز یافت می شوند (۳). چهار زیر مجموعه اصلی سیتوکروم پی ۱ تا ۴ (CYP1-4) که به نظر، مسئول بیش از ۸۰ درصد متابولیسم دارو هستند، شناسایی شده است که در آن تعداد کمی از زیر گروه ها (“ایزوفرم ها”) به عنوان آنزیم های اصلی (جدول ۴) در متابولیسم دارو درگیر هستند (۳, ۴).
جدول ۴. القاء کننده ها و مهارکننده های رایج ایزوفرم های سیتوکروم پی (۴, ۱۰, ۱۱)
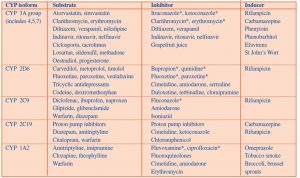
* یک مهار کننده قوی را نشان می دهد، به عنوان مثال دارویی که باعث افزایش بیش از ۵ برابری سطح پلاسما و یا کاهش بیش از ۸۰ درصدی در پاکسازی (کلریانس) می شود.
هر کدام از این آنزیم ها به تنهایی دارای سوبسترای ویژه ای هستند. به عنوان مثال داروهای متابولیزه شده توسط CYP3A4 ممکن است با سایرین تداخل داشته باشند، اما با داروهای متابولیزه شده توسط CYP2D6، تداخلی نداشته باشند. فعالیت آنزیم های CYP توسط عوامل ژنتیکی تعدیل می شود. پلی مرفیسم یا چند شکلی ژنتیکی (به عنوان مثال کاهش در فعالیت آنزیم مورد انتظار) برای بسیاری از ایزوفرم های اصلی سیتوکروم شناسایی شده است که منجر به تغییر پاسخ دارو می شود (۸). این وضعیت ممکن است بیمار را بیشتر در معرض سمیت مواد قرار دهد (۱۲). با این وجود، عوامل دیگر مانند سن، جنسیت، رژیم غذایی، مصرف الکل یا تنباکو و همچنین بیماری های مزمن نیز در فعالیت تعدیل کنندگی آنزیم های سیتوکروم دخیل هستند (۳). زیرا عملکرد CYP در تعیین مسیری که دارو توسط بدن با آن در ارتباط است بسیار مهم می باشد. هر داروی جدید باید تحت فرآیند ارزیابی قرار گیرد تا مشخص شود که آیا آنزیم های CYP در متابولیسم آن دخیل هستند یا خیر (۱۳).
اهمیت سیستم های متابولیسمیCYP در تداخلات دارویی در این واقعیت است که فعالیت این آنزیم ها می تواند توسط داروهای خاص یا مواد برون زاد مهار یا القاء گردد. این امر موجب تغییر در سطح پلاسمایی داروی تحت تأثیر قرار گرفته خواهد شد. CYP3A و CYP2D6 مسئول بیش از ۵۰ درصد از فعالیت های متابولیسمی شناخته شده دارو هستند، بنابراین تداخلات دارویی اغلب زمانی که داروهای هر یک از این گروه ها به طور همزمان تجویز گردد، دیده خواهد شد (۱۰). مهار آنزیم معمولاً به سرعت اتفاق می افتد و باعث تجمع داروی تحت تأثیر قرار گرفته و خطر بروز سمیت توسط آن خواهد شد ( به عنوان مثال افزایش سطح تئوفیلین با استفاده از سایمتیدین). القاء آنزیم ممکن است چند روز یا چند هفته طول بکشد تا به حداکثر اثر نائل شود و معمولاً کارآیی دارو تحت تأثیر را (مانند کاهش کارآیی ضد بارداری خوراکی با فنیتوئین) پس از قطع داروهای القاء کننده کاهش می دهد (۱۰). با این حال اگر متابولیت های فعال، مسئول اثرات دارو باشند، اثر معکوس ممکن است رخ دهد. مثلاً CYP2D6 کدئین را به مورفین فعال تبدیل می کند، بنابراین مهار کننده های CYP2D6 باعث کاهش اثربخشی کدئین می شوند (۱۰).
- Kaufman DW, Kelly JP, Rosenberg L, Anderson TE, Mitchell AA. Recent patterns of medication use in the ambulatory adult population of the United States: the Slone survey. Jama. 2002;287(3):337-44.
- Ko Y, Malone DC, Skrepnek GH, Armstrong EP, Murphy JE, Abarca J, et al. Prescribers’ knowledge of and sources of information for potential drug-drug interactions. Drug Safety. 2008;31(6):525-36.
- van Boxtel CJ, Santoso B, Edwards IR. Drug benefits and risks: International textbook of clinical pharmacology-revised 2nd edition: Ios Press; 2008.
- Tredger J, Stoll S. Cytochromes P450-their impact on drug treatment. HOSPITAL PHARMACIST-LONDON-. 2002;9(6):167-73.
- Baxter K. Stockley’s Drug Interactions 9: London: Pharmaceutical Press; 2012.
- Murphy R, Grehan G, Hays V, Freeman G, Kerr P, Fahy S. Medicines management audit cycle, St. Brigid’s Hospital Ballinasloe. Irish Journal of Psychological Medicine. 2015;32(2):219-25.
- Leendertse AJ, Egberts AC, Stoker LJ, van den Bemt PM. Frequency of and risk factors for preventable medication-related hospital admissions in the Netherlands. Archives of internal medicine. 2008;168(17):1890-6.
- Enna S. Goodman & Gilman’s The Pharmacological Basis of Therapeutics Edited by Joel G. Hardman, Lee E. Limbird, Perry B. Molinoff, and Raymond W. Ruddon. McGraw-Hill, New York. 1996. xxi+ 1905 pp. 21× ۲۶ cm. ISBN 0-07-026266-7. $89.00. ACS Publications; 1997.
- Gilman A, Hardman J, Limbird L. Goodman and Gilman’s, the Pharmacological basis of erapeutics. McGraw-Hill, New York, NY, USA; 2001.
- Wilkinson GR. Drug metabolism and variability among patients in drug response. New England Journal of Medicine. 2005;352(21):2211-21.
- Flockhart D. Drug interactions: Cytochrome P450 Drug Interaction Table. Indiana School of Medicine 2007. 2007.
- Phillips KA, Veenstra DL, Oren E, Lee JK, Sadee W. Potential role of pharmacogenomics in reducing adverse drug reactions: a systematic review. Jama. 2001;286(18):2270-9.
- Bordia A, Sanadhya S, Rathore A, Bhu N. Essential oil of garlic on blood lipids and fibrinolytic activity in patients of coronary artery disease. Part I. The Journal of the Association of Physicians of India. 1978;26(5):327-31.